O que é alotropia com exemplos do oxigênio e carbono
Alotropia é o fenômeno onde um elemento químico é capaz de originar duas ou mais substâncias simples diferentes. Veja exemplos e resolva exercícios de como essas questões podem cair na sua prova.
Antes de começarmos a falar sobre alotropia, precisamos lembrar de um conceito bem simples e introdutório da Química. A união de átomos iguais forma o que chamamos de substâncias simples.
A partir disso, estudamos a alotropia, que é um fenômeno químico onde um elemento químico é capaz de originar duas ou mais substâncias simples diferentes.
Alguns elementos químicos são capazes de formar substâncias simples diferentes. Como por exemplo temos os elementos oxigênio, carbono, fósforo e enxofre que estudaremos nessa aula.
Estes elementos químicos apresentam diferenciação de acordo com a quantidade de átomos da molécula e pela sua estrutura. Suas propriedades físicas são diferentes e as propriedades químicas são bastante semelhantes.
Alotropia do oxigênio
O elemento químico oxigênio pode ligar-se a outro átomo de oxigênio, formando o gás oxigênio (O2). Ou também pode ligar-se a 2 outros átomos de oxigênio formando o ozônio (O3).
Sabemos que o gás oxigênio é incolor e inodoro, importante no processo de respiração celular e atua no processo de combustão.
Já o ozônio é um gás azulado que protege contra a radiação ultravioleta, que é nociva aos seres vivos. Quando se encontra na atmosfera, ele é considerado um poluente. Pode ser usado também no lugar do cloro em filtros e piscinas, melhorando a qualidade da água.
O ozônio não causa ardência nos olhos e promove a eliminação de microrganismos presentes na água.
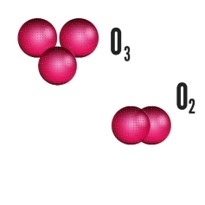 Representação do oxigênio (O2) e do ozônio (O3).
Representação do oxigênio (O2) e do ozônio (O3).
Sempre há um elemento mais estável (e consequentemente mais abundante) do que o outro. Então como podemos saber quem será o mais estável?
O mais estável será aquele que ocorre em maior quantidade no nosso planeta. Fica fácil perceber entre as duas formas alotrópicas de oxigênio qual é o mais estável: o gás oxigênio (O2) é o mais estável, pois representa cerca de 20% da atmosfera.
Podemos dizer que as formas alotrópicas do oxigênio diferem pela atomicidade.
Outros elementos químicos e alotropia
Outro elemento que apresenta formas alotrópicas é o carbono. Este apresenta 3 formas diferentes: Cn (grafite), Cn (diamante) e C60 (fulereno).
O carbono grafite é formado por anéis hexagonais ligados entre si, por meio de ligações frágeis, formando camadas sobrepostas que deslizam com facilidade. É bem macio, por isso, quando escrevemos fica registrado no papel. O grafite conduz eletricidade e pode ser usado também como lubrificante.
O carbono diamante é tridimensional, onde os carbonos estão ligados uns aos outros formando uma organização muito rígida. Tem o formato de tetraédrico e não conduz corrente elétrica.
O fulereno (C60) é uma descoberta recente com um total de 60 átomos de carbono! Seu aspecto assemelha-se a uma bola de futebol. É macio e conduz eletricidade.
A mais estável é o carbono grafite.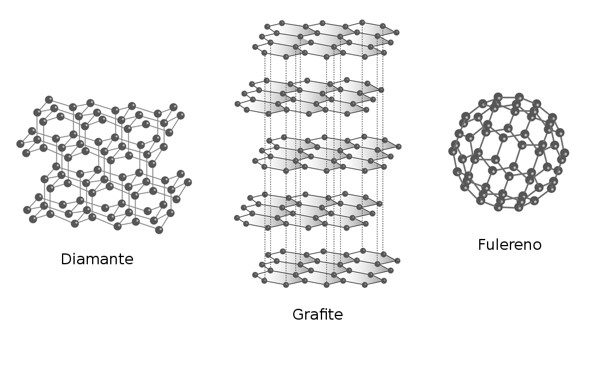
Podemos dizer que as formas alotrópicas do carbono diferem quanto a sua estrutura.
O fósforo também apresenta 2 formas alotrópicas, o P4 e o PN.
O fósforo P4 (fósforo branco com 4 átomos) é muito reativo e extremamente tóxico. Sofre combustão espontaneamente em contato com o ar. Ele é usado na fabricação de bombas.
O fósforo PN (vermelho) é uma macromolécula, formada por várias estruturas de fósforo branco repetidas, por isso a letra N. Este não sofre combustão espontânea em contato com o ar. É usado na fabricação de caixas de fósforos.
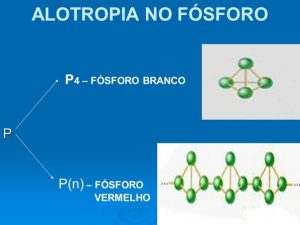 Alotropia do Fósforo. Fonte: slideplayer.com.br
Alotropia do Fósforo. Fonte: slideplayer.com.br
Podemos dizer que as formas alotrópicas do fósforo diferem quanto sua atomicidade. A forma mais estável do fósforo é o PN.
O elemento enxofre apresenta duas formas alotrópicas: S8(rômbico) e o S8(monoclínico). A diferença entre estas duas estruturas é seu arranjo cristalino. O mais abundante é o Rômbico.
 Alotropia do fósforo. Fonte: manualdaquimica.com.br
Alotropia do fósforo. Fonte: manualdaquimica.com.br
Resumo
Veja a aula abaixo, com a professora Larissa, do Curso Enem Gratuito, e confira as principais dicas sobre o que é alotropia:
Exercícios sobre Alotropia
1) (CFTMG)
“No Brasil, o câncer mais frequente é o de pele, sendo que o seu maior agente etiológico é a radiação ultravioleta (UV) proveniente do sol. Em decorrência da destruição da camada de ozônio, os raios UV têm aumentado progressivamente sua incidência sobre a terra.”
(Texto adaptado no INCA, 2009)
Em relação ao ozônio, afirma-se, corretamente, que é
a) alótropo do O2, por ser formado pelo mesmo elemento químico.
b) isóbaro do monóxido de enxofre porque possuem a mesma massa.
c) isótopo do gás oxigênio, pois ambos têm o mesmo número atômico.
d) substância pura composta, uma vez que se constitui de 3 átomos de oxigênio.
2) (Ufpb)
Em 1996, o prêmio Nobel de Química foi concedido aos cientistas que descobriram uma molécula com a forma de uma bola de futebol, denominada fulereno (C60). Além dessa substância, o grafite e o diamante também são constituídos de carbono. Os modelos moleculares dessas substâncias encontram-se representados abaixo.
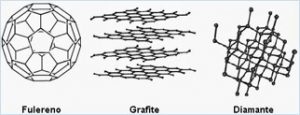
A respeito dessas substâncias, é correto afirmar:
a) O grafite e o diamante apresentam propriedades físicas idênticas.
b) O fulereno, o grafite e o diamante são substâncias compostas.
c) O fulereno, o grafite e o diamante são isótopos.
d) O fulereno, o grafite e o diamante são alótropos.
e) O fulereno é uma mistura homogênea de átomos de carbono.
3) (UNESP SP)
Os recém-descobertos fulerenos são formas alotrópicas do elemento químico carbono. Outras formas alotrópicas do carbono são:
a) isótopos de carbono-13.
b) calcário e mármore.
c) silício e germânio.
d) monóxido e dióxido de carbono.
e) diamante e grafite.
4) (UFAL)
Alotropia é um fenômeno relacionado com:
a) substâncias simples
b) substâncias iônicas
c) compostos binários
d) elementos químicos metálicos
e) substâncias orgânicas oxigenadas
5) (PUC-PR)
Assinale a alternativa correta:
a) variedades alotrópicas são substâncias compostas formadas pelos mesmos elementos químicos
b) formas alotrópicas de um mesmo elemento apresentam propriedades físicas diferentes
c) H2O e H2O2 são formas alotrópicas
d) gás oxigênio (O2) e gás ozônio (O3) são substâncias compostas
e) a forma alotrópica mais estável é a que contém maior quantidade de energia armazenada
Gabarito:
- A
- D
- E
- A
- B





