O que é energia térmica e sua relação com calor e temperatura
O que é calor? Qual a diferença entre calor e temperatura? O que é caloria? Qual a relação entre caloria e joule? Quais são os estados de agregação da matéria?
Nessa aula você irá rever tudo sobre calor e energia térmica. Saberá diferenciar calor de temperatura e entenderá porque é medido em caloria e Joule. Você também irá rever o conceito de equilíbrio térmico e o que acontece com os estados da matéria quando recebem energia após um certo limite. Revise energia com esta aula de física para mandar bem no Enem e nos vestibulares!
Energia térmica
Imagine que você está em uma minúscula nave entrando no corpo humano. Você verá muitos órgãos, e olhando somente para um, verá que é formado por tecidos. Olhando mais de perto, verá as células e, chegando mais perto ainda, verá as moléculas. As moléculas, essas pequeníssimas partes que constituem toda a matéria, inclusive nosso corpo, é o que nos interessam nesta aula.
As moléculas constituintes não só dos tecidos, mas de todo matéria existente estão sempre em movimento. Esse movimento é denominado agitação térmica. A energia associada a esse movimento recebe o nome de energia térmica.
Essa energia pode variar para mais ou para menos. Por exemplo: se você coloca um pouco de água no fogo, observará que ela esquenta. Nesse caso, suas moléculas ficam mais agitadas. Ao passo que ao colocar algumas pedras de gelo nela, verás que ela esfria. Nesse momento, elas ficarão menos agitadas.
Podemos concluir que a energia térmica de um corpo se transferiu para outro, no caso do fogo para a água. Ou, da água para o gelo. Quando a água esquentou, ela recebeu energia ao passo que, quando esfriou, ela cedeu energia para o gelo.
O esquenta e esfria são apenas sensações de nosso tato e não grandezas físicas passiveis de serem analisadas e quantificadas. Por isso, temos que ter cuidado ao observá-las. Na verdade, o que está ocorrendo é uma transferência de calor.
O que é calor?
Podemos definir calor como uma forma de energia, melhor ainda, energia em trânsito, pois sempre está se movimentando.
A medida da quantidade de calor trocada entre corpos é também uma medida de energia. Por essa razão a unidade de medida de quantidade de calor no Sistema Internacional é o Joule (J).
Entretanto, também encontramos ela sendo medida como caloria (cal). É muito importante você saber a relação de equivalência entre essas duas medidas pois é muito requisitada em vestibulares.
1 cal = 4,1868 J
Temperatura
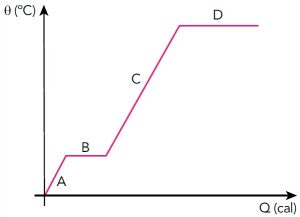
Analisando o que acontece com a água enquanto recebe calor e não muda de fase, observamos que sua temperatura aumenta, pois, as moléculas aumentam seu movimento. E, quando perde energia, suas moléculas diminuem esse movimento, então sua temperatura diminui.
Então, podemos definir temperatura como o grau de agitação dessas moléculas.
Equilíbrio térmico
Essa transferência de energia entre dois ou mais corpos acontece até que eles estejam na mesma temperatura, ou seja, suas moléculas estiverem no mesmo grau de agitação.
Quando esse grau comum for alcançado não haverá mais troca de energia térmica. Esse estado é denominado equilíbrio térmico.
Agora, vejamos como esse grau de agitação das moléculas caracteriza os estados da matéria.
Grau de agitação térmica e estados físicos da matéria
Temos os estados sólido, líquido e gasoso. Em geral, todos os materiais que nos rodeiam se encontram em um desses estados.
A matéria no estado sólido possui volume e forma bem definida. No estado líquido, a matéria não tem forma e assume aquela do recipiente que o contém, mas possui volume definido. Já no estado de gás ou vapor (deixamos para falar a respeito da diferença entre eles em outro post), a matéria não possui forma definida, porém, ocupa totalmente aquela do recipiente que o contém. Portanto não possui também volume definido.
Para concluir, dizemos que a força de coesão existente entre as moléculas age oposta ao seu movimento.
- Se a força de coesão é grande, temos o estado sólido, pois a agitação de moléculas nesse estado é pequena.
- Se a força de coesão é média, temos o estado líquido, uma vez que há movimentação razoável, porém limitada.
- Se a força de coesão é pequena, temos o estado gasoso, com movimentação muito intensa. Por essa razão, os gases se difundem por todo o espaço em que se encontram.
Mudanças de fase
A mudança de um estado para outro da matéria depende da quantidade de energia que se ganha ou que se perde. Por exemplo, a água em sua forma líquida, quando muito aquecida, muda de fase, virando vapor.
Acompanhe no esquema abaixo os nomes das mudanças de fase:
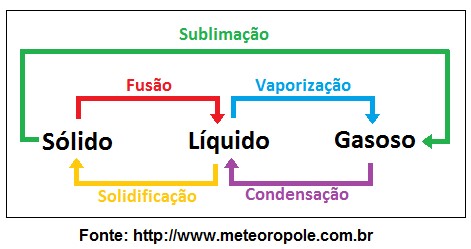
- Sublimação: Do sólido para o gasoso. Exemplo: Naftalina
- Fusão: Sólido para líquido
- Vaporização: Líquido para gasoso
- Condensação: Gasoso para líquido
- Solidificação: Líquido para sólido.
Vale lembrar que evaporação e ebulição são formas para se conseguir a vaporização.
Videoaula
Para aprofundar seus estudos, confira a aula do prof. Tonho no nosso canal:
Exercícios sobre energia térmica
Agora resolva 10 exercícios sobre energia térmica e continue estudando:
Sumário do Quiz
0 de 10 questões completadas
Perguntas:
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
Information
.
Você já fez este questionário anteriormente. Portanto, não pode fazê-lo novamente.
Quiz is loading...
You must sign in or sign up to start the quiz.
Para iniciar este questionário, você precisa terminar, antes, este questionário:
Resultados
0 de 10 perguntas respondidas corretamente
Seu tempo:
Acabou o tempo
Você conseguiu 0 de 0 pontos possíveis (0)
| Pontuação média |
|
| Sua pontuação |
|
Categorias
- Sem categoria 0%
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- Respondido
- Revisão
-
Pergunta 1 de 10
1. Pergunta
(ENEM/2017)
Alguns fenômenos observados no cotidiano estão relacionados com as mudanças ocorridas no estado físico da matéria. Por exemplo, no sistema constituído por água em um recipiente de barro, a água mantém-se fresca mesmo em dias quentes.
A explicação para o fenômeno descrito é que, nas proximidades da superfície do recipiente, a
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 2 de 10
2. Pergunta
(IFSC/2016)
A matéria pode se apresentar, basicamente, em três estados físicos: sólido, líquido e gasoso. Sabemos que a matéria pode mudar de estado, dependendo do fornecimento ou retirada de energia.
Assinale a alternativa CORRETA.
Quando uma substância está no estado líquido e muda para o gasoso, dizemos que ela sofreuCorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 3 de 10
3. Pergunta
(UFRR/2015)
Um professor de Física pede aos seus alunos que façam um trabalho referente a fluidos. Um deles procura na internet e encontra um vídeoaula referente a fluidos, ele assiste e faz as seguintes anotações.
I. um corpo sólido tem geralmente volume e forma bem definidos, que só se alteram em resposta à força externa;
II. um líquido tem volume bem definido, mas não a forma: mantendo o seu volume, amolda-se ao recipiente que o contém;
III. um gás não tem nem forma nem volume bem definido, expandindo-se até ocupar todo o volume do recipiente que o contém;
IV. todos os estados da matéria podem ser considerados como fluidos;
V. quando o fluido está em repouso, ele exerce uma força paralela sobre qualquer superfície que esteja em contato com ele.Analisando as anotações I, II, III, IV e V do aluno, assinale a alternativa esta correta:
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 4 de 10
4. Pergunta
(UEA AM/2014)
É possível passar a matéria do estado sólido diretamente para o gasoso, evitando a fase líquida. Tal fenômeno físico se verifica comumente no gelo seco e na naftalina, mas também pode ocorrer com a água, dependendo das condições de temperatura e pressão. A essa passagem dá-se o nome de
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 5 de 10
5. Pergunta
(UFPel RS/2014)
No ciclo da água, temos a presença dos três estados da matéria, o sólido, o líquido e o gasoso, conforme mostra a charge.

Fonte: Maurício de Souza
Em relação às mudanças de estado da matéria no ciclo da água, é correto afirmar que
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 6 de 10
6. Pergunta
(UNISC RS/2011)
Fenômenos físicos nos rodeiam. Todos os dias, a todo o momento, nos deparamos com alterações de toda a ordem. A evaporação da água do mar, a condensação do vapor d’água na forma de nuvens e de chuva ou a solidificação da água em granizo ou em neve são exemplos de
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 7 de 10
7. Pergunta
(ENEM/2016)
Nos dias frios, é comum ouvir expressões como: “Esta roupa é quentinha” ou então “Feche a janela para o frio não entrar”. As expressões do senso comum utilizadas estão em desacordo com o conceito de calor da termodinâmica. A roupa não é “quentinha”, muito menos o frio “entra” pela janela.
A utilização das expressões “roupa é quentinha” e “para o frio não entrar” é inadequada, pois o(a)
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 8 de 10
8. Pergunta
(IFRS/2015)
A respeito dos fenômenos térmicos, analise as afirmações a seguir.
I. Em locais muito frios, é conveniente a instalação de sistemas de calefação para aquecer os ambientes. É recomendado que esse sistema seja instalado na parte superior da parede do ambiente para que o ar quente possa circular com mais facilidade.
II. Quando as mãos são atritadas, aumenta a energia cinética das moléculas em fricção, o que provoca uma elevação de temperatura das mãos.
III. Equilíbrio térmico é a situação caracterizada pela igualdade entre a temperatura dos corpos em contato.
IV. Calor é a energia transferida de um corpo para o outro em função da diferença de temperatura entre esses corpos.
V. O conceito de calor está relacionado com a sensação térmica, ou seja, um dia em que a temperatura ambiente está em torno de 36º C, apresenta um alto índice de calor.Estão corretas apenas
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 9 de 10
9. Pergunta
(UNIUBE MG/2014)
Um aluno empolgado com os conceitos estudados na aula de Física colocou uma pequena quantidade de água para aquecer no fogão. Quando a água começou a ferver, ele desligou o fogo e, cuidadosamente, aspirou uma porção de água para o interior de uma seringa sem agulha. Após um tempo, o aluno percebeu que a água na seringa havia parado de ferver. Ele então tapou com um dos dedos a entrada de água na seringa, puxou o êmbolo, e observou que a porção de água no interior da seringa havia voltado a ferver. Tal fato somente é possível devido:
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!
-
Pergunta 10 de 10
10. Pergunta
(UEG GO/2013)
Alguns conceitos de física aparecem comumente no cotidiano e são equivocadamente interpretados. Com relação a esse fato, o conceito correto é o seguinte:
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta. Veja uma revisão nesta aula e continue se preparando para o Enem e vestibulares!

Sobre o(a) autor(a):
Rodinei Pachani - Rodinei Pachani é mestre em Geofísica pela USP-SP, com licenciatura plena em matemática, possui pós-graduação em Gerência Financeira e especialização em Estatística Aplicada. Possui experiência de mais de 28 anos em sala de aula, tendo trabalhado com ensino médio, cursinhos e Faculdades. É autor do livro “Ciência ao alcance de todos” e possui um canal no YouTube onde realiza experimentos, explica conteúdos e resolve exercícios de física.
Gostou? Compartilhe!
Continue lendo:
Aqui vão 2 publicações relacionadas que talvez você goste:

Corrente elétrica: o que é e como calcular sua intensidade
Por Ana Carolina Prieto | 10 de julho
O que é corrente elétrica? A corrente elétrica flui do polo negativo ou do positivo de uma pilha? Qual a...

As Leis de Newton: os princípios da mecânica clássica
Por Martha Ramos | 18 de março
As leis de Newton constituem um dos temas mais importantes da Física e sempre são cobradas no Enem e nos...


