Veja as propriedades químicas da matéria
Aprenda nesta aula todas as propriedades químicas da matéria, desde as propriedades gerais até às específicas. Prepare-se para a prova do Enem e dos vestibulares com a gente!
A matéria passa por inúmeras transformações na natureza, sendo formada por partículas muito pequenas denominadas átomos. Para podermos identificar os materiais, saber sua composição, características e outras denominações, devemos estudar e analisar as propriedades químicas da matéria.
Para isso, dividimos as propriedades em dois tipos. As propriedades gerais são comuns à todo tipo de matéria, não identificando uma substância.
Já as propriedades específicas servem para identificar os materiais, destacando suas características específicas.
O que é a matéria? – Veja agora com a professora Larissa Campos, do canal do Curso Enem Gratuito:
Propriedades gerais e específicas da matéria
As propriedades gerais da matéria estão relacionadas com a massa e o volume. Elas ocorrem em todo tipo de matéria, como a extensão, inércia, elasticidade (onde os corpos podem voltar as suas formas e volumes iniciais), a impenetrabilidade (dois corpos não ocupam o mesmo lugar no espaço ao mesmo tempo) e a divisibilidade (corpos podem ser divididos em partes menores).
As propriedades específicas servem para identificar os materiais e são divididas em físicas, organolépticas e químicas. As primeiras (físicas e organolépticas) já foram estudadas em outra aula de nosso site, agora vamos entender o que são as propriedades químicas da matéria.
As propriedades químicas da matéria
Estão relacionadas com as transformações químicas, onde ocorre mudança na composição da matéria.
Essas mudanças de composição ocorrem por meio de uma reação química, originando novas substâncias. Essas transformações envolvem energia, que pode ser liberada ou absorvida pelo sistema.
Veja as Propriedades Físicas e Químicas da Matéria
As propriedades químicas ocorrem em certas reações químicas como a combustibilidade, que representa o efeito de queimar em um processo de combustão.
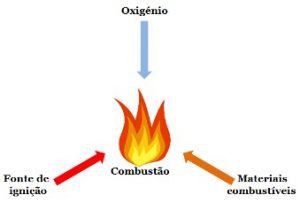
Para que o processo de combustão ocorra devem estar presentes: combustível, que é um material inflamável, volátil, que evapora com facilidade, como por exemplo o álcool, madeira, querosene, gás de cozinha; o comburente, que é a substância que alimenta a combustão, temos como exemplo o gás oxigênio, e o calor ou uma fonte de ignição.
Outra propriedade química muito importante é a reatividade, que representa a facilidade dos átomos em interagirem com outras substâncias.
Há elementos que reagem com grande facilidade para adquirir estabilidade química, como é o caso do Hidrogênio molecular (H2), que participa de reações como a de combustão.
Outros elementos são pouco reativos, como os gases nobres, que não realizam reações químicas com outros átomos com facilidade, podendo ser encontrados sozinhos. Os 6 gases nobres são encontrados isolados porque atingiram a estabilidade na última cada da eletrosfera: contam com 8 elétrons na mesma.
A toxicidade representa a capacidade do elemento químico ou substância ser nocivo a um organismo, provocando efeitos colaterais indesejáveis.
Temos também a propriedade explosibilidade, que é a capacidade de sofrer explosão, mudando sua estrutura química, como exemplo temos o gás hidrogênio, altamente explosivo e o TNT.
Oxidação e corrosão
Outra propriedade química importante é a oxidação, presente em nosso dia a dia, onde todos os materiais podem sofrer este processo, por causa do contato dos materiais com o ar atmosférico e a umidade.
A oxidação representa a perda de elétrons e origina a corrosão e a ferrugem.
O oxigênio e a umidade se combinam para provocar a ferrugem e a corrosão dos materiais. Nós vemos isso acontecendo com frequência já que o ferro é o metal mais usado pelo homem e ele se corrói com muita facilidade.
A corrosão é o desgaste do material (metal) a partir da oxidação quando fica mais exposto aos danos causados pelo contato com a atmosfera, abrindo um buraco na superfície do metal.
Isso ocorre, por exemplo, quando instalamos telas para gatos e crianças nos apartamentos. Se você optar pelo gancho de metal, tenha em mente que ele sofrerá com a corrosão e a oxidação ao longo do tempo. E em um período de alguns anos você terá que trocar o material.
Para retardar os efeitos da corrosão deve-se utilizar uma proteção de contato como tintas e vernizes para cobrir a superfície e isolar o ferro.

Ferrugem
No processo de ferrugem, os materiais já estão oxidados, principalmente os metais ferrosos, e começam a produzir o hidróxido de ferro, a camada avermelhada que caracteriza o processo da ferrugem.
Para se evitar a oxidação pode-se usar um metal de sacrifício, que irá atuar sobre o material de ferro. Este metal irá perder elétrons e será corroído, precisando ser reposto.
Outra técnica também é o uso da folha de flandres nas latas de ferro, que são revestidas com um metal mais nobre, como o estanho, que impede a oxidação do ferro.
Um cuidado importante é observar se as latas não se encontram amassadas, pois se elas estiverem amassadas, isso pode quebrar o estanho.
Assim o ferro acaba ficando exposto e, consequentemente, o oxigênio e a água atacarão o ferro. Esse fenômeno causará a oxidação, alterando a composição do produto no interior da lata.
O processo de oxidação também ocorre no nosso organismo, pois necessitamos do oxigênio para sobreviver. O oxigênio oxida nosso corpo, provocando seu envelhecimento!
É por isso que existem inúmeros cremes anti-envelhecimento, que formam uma camada protetora na pele, para atenuar ou prevenir a oxidação.
Outro processo que ocorre no nosso cotidiano é o escurecimento dos alimentos. Você já deve ter observado que se deixar uma banana sem casca exposta ao ar, ela irá escurecer. O oxigênio do ar também oxida a matéria orgânica dos alimentos!
Viu como a química e as propriedades químicas da matéria estão presentes em vários momentos da nossa vida?!
Exercícios sobre Propriedades Químicas da Matéria:
1) (CFT-PR)
As propriedades de um material utilizadas para distinguir-se um material do outro são divididas em Organolépticas, Físicas e Químicas. Associe a primeira coluna com a segunda coluna e assinale a alternativa que apresenta a ordem correta das respostas.

a) A, B, C, C, B, A, B.
b) A, B, C, A, B, C, B.
c) A, C, B, C, B, C, B.
d) A, B, C, B, B, A, B.
e) C, B, A, C, B, A, B.
Gabarito: A
2) (VUNESP)
Indicar a alternativa que representa um processo químico.
a) dissolução de cloreto de sódio em água
b) fusão da aspirina
c) destilação fracionada do ar líquido
d) corrosão de uma chapa de ferro
e) evaporação da água do mar
gabarito: D





