As substâncias simples, compostos, misturas e sistemas
As substâncias e os sistemas são fundamentais para você entender a Química e ir bem nas provas. Estude com nossa aula e resolva os exercícios no final!
As substâncias representam um material que possui propriedades bem definidas, sendo formadas por moléculas iguais. Cada molécula pode ser formada por um grupo de átomos de mesmo elemento químico ou por elementos químicos diferentes.
Sabemos que a matéria é formada por átomos, que ocupa lugar no espaço e apresenta massa. Essa pode ser encontrada no estado sólido, líquido e gasoso.
Os átomos se ligam para formar compostos, porque atingem sua estabilidade, e dependendo de como as substâncias são formadas elas podem ser classificadas em simples e compostas.
A classificação das substâncias e sistemas
Veja ese resumo de introdução ao tema com o professor Felipe Sobis, da disciplina de química do Curso Enem Gratuito::
A Classificação das substâncias
Os átomos podem se unir com átomos de mesmo elemento químico e teremos a formação de uma substância simples. Como exemplo de substância simples temos o gás oxigênio (O2), o gás nitrogênio (N2).
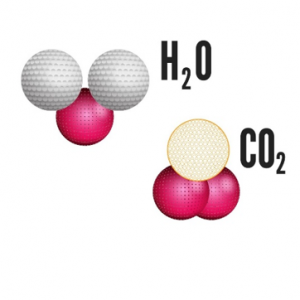
Os átomos também podem se unir com átomos diferentes, formando as substâncias compostas. Como exemplo temos as fórmulas: H2O; CO2; NH3.
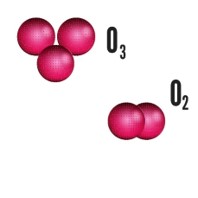
Nas substâncias simples ocorre o processo de alotropia, onde um mesmo elemento origina substâncias diferentes. Como exemplo deste processo podemos citar o oxigênio, que pode formar o gás oxigênio (O2), que é incolor, participa do processo de combustão e atua no metabolismo celular.
E pode formar também o ozônio (O3), um gás azulado, bactericida e tóxico.
O que são misturas
Duas ou mais substâncias diferentes podem se unir e formar uma mistura. As misturas podem ocorrer nos estados sólido, líquido e gasoso e não definem fórmulas.
Como exemplo podemos citar o ar atmosférico, água mineral, bronze, etc. As misturas podem ser classificadas em homogêneas e heterogêneas.
As misturas homogêneas apresentam apenas uma fase e não ocorre distinção entre seus componentes. São classificadas como monofásicas. Como exemplo temos um copo com água e um pouco de açúcar, misturamos bem e não podemos verificar onde está o açúcar ou a água, pois visualizamos uma estrutura única.
Resumo sobre as Misturas
Veja com o professor Felipe Sobis as dicas básicas sobre as Misturas para gabaritar as questões de Química nas provas.
As misturas homogêneas são denominadas de solução. Confira na imagem, e veja na explicação:
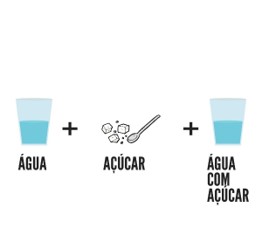
As misturas heterogêneas apresentam duas ou mais fases, e conseguimos identificar cada fase do sistema. São classificadas como polifásicas.
Por exemplo podemos citar um copo com água e óleo, onde observamos onde se localiza a água e onde se localiza o óleo. O granito é um exemplo também de mistura heterogênea, pois ele é formado por 3 fases: quartzo, feldspato e mica, e apresenta também 3 componentes.
A fase representa cada porção visível do sistema.
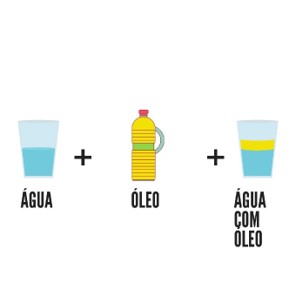
Em recipientes fechados, a fase gasosa deve ser considerada. Por exemplo, em uma garrafa fechada com água e uma parte vazia. Neste caso teremos 2 fases, que representam a fase líquida e a fase gasosa.
Alguns sistemas parecem ser homogêneos a olho nu, mas ao microscópio mostram desigualdades. É o caso do leite, do sangue e a maionese.
O que são os sistemas
O sistema representa uma porção que serve para ser analisado, como um copo contendo água, um pedaço de madeira, etc. O sistema é formado pela mesma substância.
Os sistemas podem ser homogêneos, como um copo com água, e heterogêneos, como um copo contendo água e um cubo de gelo. Note que este é formado por 2 fases diferentes (líquida e sólida) e um único componente.
Vamos identificar alguns tipos de misturas?
Na mistura água + óleo, observamos que o óleo permanece na superfície do recipiente e a água está na parte inferior. Temos neste exemplo uma mistura, formada por 2 substâncias diferentes, com 2 fases distintas e 2 componentes.
Na mistura água + areia, observamos que a areia permanece no fundo do recipiente, então teremos uma mistura formada por 2 fases e 2 componentes.
Na mistura água + sal, nós não conseguimos distinguir onde o sal está, pois ele foi totalmente dissolvido no recipiente. Neste caso teremos uma mistura homogênea formada por 1 fase e 2 componentes.
Na mistura água + óleo + gelo, teremos 3 fases e 2 componentes, pois o gelo é água, o mesmo ocorrendo na mistura água gaseificada + gelo, onde também teremos 3 fases e 2 componentes.
Na mistura água + sal + óleo + gelo + granito, teremos 6 fases e 6 componentes. Onde o granito é formado por 3 elementos diferentes e a mistura: água e sal formam um só componente.
Exercícios sobre substâncias
Sumário do Quiz
0 de 10 questões completadas
Perguntas:
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
Information
.
Você já fez este questionário anteriormente. Portanto, não pode fazê-lo novamente.
Quiz is loading...
You must sign in or sign up to start the quiz.
Para iniciar este questionário, você precisa terminar, antes, este questionário:
Resultados
0 de 10 perguntas respondidas corretamente
Seu tempo:
Acabou o tempo
Você conseguiu 0 de 0 pontos possíveis (0)
| Pontuação média |
|
| Sua pontuação |
|
Categorias
- Sem categoria 0%
- 1
- 2
- 3
- 4
- 5
- 6
- 7
- 8
- 9
- 10
- Respondido
- Revisão
-
Pergunta 1 de 10
1. Pergunta
(IFSC/2015)
Os veículos automotores emitem gases poluentes na atmosfera como o NO2 e o NO3, conhecidos pelos nomes de óxido nitroso e óxido nítrico, respectivamente, os quais reagem com a água da chuva precipitando na forma de ácido nítrico. Já o SO2, precipita na forma de ácido sulfúrico também quando reage com a água da chuva. Esses ácidos são altamente tóxicos e corrosivos: nos vegetais retardam o crescimento, e nos seres humanos atacam as vias respiratórias.
A respeito dessas substâncias poluentes grifadas no texto e os elementos químicos que a constituem, é CORRETO afirmar que:
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 2 de 10
2. Pergunta
(PUC RS/2015)
Analise as informações a seguir.
Durante séculos, filósofos e alquimistas acreditaram que a matéria era constituída de quatro elementos fundamentais: terra, água, ar e fogo. Hoje, contudo, reconhecemos a existência de muito mais do que quatro elementos e alcançamos uma compreensão mais aprofundada sobre o que, de fato, são água, ar, terra e fogo.
Sobre esse assunto, são feitas as seguintes afirmativas:
I. A água é uma substância simples.
II. O ar é uma solução.
III. A terra é uma mistura heterogênea.
IV. O fogo é uma reação redox endotérmica.São corretas somente as afirmativas
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 3 de 10
3. Pergunta
(UNIFOR CE/2015)
A imagem abaixo ilustra um pacote de um produto comercial vendido como fertilizante e conhecido como NPK. As siglas NPK são uma referência à química e especificamente a presença dos elementos químicos componentes deste material.

Os elementos químicos em questão são, respectivamente:
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 4 de 10
4. Pergunta
(Unimontes MG/2008)
Um tubo de ensaio é imerso de cabeça para baixo num recipiente com água. Observa-se que a água adentra o interior do tubo de ensaio até um certo nível, como ilustra a figura:
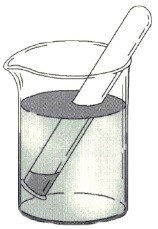
A água não preenche completamente o tubo porque
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 5 de 10
5. Pergunta
(UNIRIO RJ/2007)
“… a biodegradação pode não ocorrer com a rapidez necessária e os ambientes aquáticos tornam-se anaeróbios (reduzido teor de oxigênio dissolvido), passando a exalar cheiro desagradável, com formação de gás sulfídrico (ácido sulfídrico), e de outros produtos da atividade microbiana (…) tais como íons acetato e os gases hidrogênio, carbônico e metano”.
Ciência Hoje, 2005
Entre os compostos citados, classificam-se como substâncias simples
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 6 de 10
6. Pergunta
(UEA AM/2016)
Desinfetante de amplo uso nas residências, a água sanitária é um exemplo de
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 7 de 10
7. Pergunta
(Unievangélica GO/2015)
Considera-se um sistema homogêneo ou heterogêneo qualquer porção do universo que seja submetido a uma observação, sendo que a mesma pode ser uma substância pura ou uma mistura.
São exemplos de sistemas homogêneos e heterogêneos, respectivamente,
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 8 de 10
8. Pergunta
(FGV SP/2013)
A química é responsável pela melhora em nossa qualidade de vida e está inserida em nosso cotidiano de muitas formas em substâncias e misturas que constituem diversos materiais.
Assinale a alternativa que apresenta, respectivamente, substância simples, substância composta, mistura homogênea e mistura heterogênea.CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 9 de 10
9. Pergunta
(UEL PR/2007)
Um rapaz pediu sua namorada em casamento, presenteando-a com uma aliança de ouro 18 quilates. Para comemorar, sabendo que o álcool é prejudicial à saúde, eles brindaram com água gaseificada com gelo, ao ar livre. Os sistemas: ouro 18 quilates, água gaseificada com gelo e ar atmosférico, são, respectivamente:
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.
-
Pergunta 10 de 10
10. Pergunta
(Mackenzie SP/2006)
Não é exemplo de mistura:
CorretoParabéns, resposta correta! Siga com o simulado.
IncorretoA resposta está incorreta.

Sobre o(a) autor(a):
Roseli Prieto - Texto elaborado por Roseli Prieto, professora de Química e Biologia da rede estadual de São Paulo. Já atuou em diversas escolas públicas e privadas de Santos (SP). É Gestora Ambiental e Especialista em Planejamento e Gestora de cursos a distância.
Gostou? Compartilhe!
Continue lendo:
Aqui vão 2 publicações relacionadas que talvez você goste:

PodPassarEnem o videocast Curso Enem Gratuito
Por Jaqueline Padilha | 20 de maio
Se você estava procurando um videocast para estudar para o Enem de forma mais leve e contextualizada, acabou de encontrar....

Aulão Enem de Química: revisão intensiva e gratuita para a prova
Por João Vianney dos Valles Santos | 11 de outubro
Assista ao Aulão Enem de Química do Curso Enem Gratuito e revise os conteúdos mais importantes para a prova.


